题记:本文主要介绍生存资料处理的Fine-Gray检验与竞争风险模型,在生存资料处理中,这种方法目前应用越来越广泛。
1. 背景知识
在观察某事件是否发生时,如果该事件被其他事件阻碍,即存在所谓“竞争风险”。研究中结局事件可能有多个,某些结局将阻止感兴趣事件的出现或影响其发生的概率,各结局事件形成“竞争”关系,互为竞争风险事件。
举例来说,某研究人员收集了本市2007年确诊为轻度认知损害(MCI)的518例老年患者临床资料,包括基本人口学特征、生活方式、体格检查和合并疾病信息等,并于2010~2013年完成6次随访调查,主要观察结局为发生阿尔兹海默病(AD)。随访期间,共发生AD78例,失访84例,其中28例搬迁、31例退出、25例死亡。试问影响MCI向AD转归的因素都有哪些?本例中,如果MCI患者在观察期间死于癌症、心血管疾病、车祸等原因而未发生AD,就不能为AD的发病做出贡献,即死亡“竞争”了AD的发生。传统生存资料统计方法将发生AD前死亡的个体、失访个体和未发生AD个体均按删失数据(censored data)处理,可能会导致估计偏差[1]。对于死亡率较高的老年人群,当有竞争风险事件存在时,采用传统生存分析方法(K-M法、Cox比例风险回归模型)会高估所研究疾病的发生风险,产生竞争风险偏倚,有人专门研究发现约46%的文献可能存在这种偏倚。
本例中若选用竞争风险模型处理较为恰当。所谓竞争风险模型(Competing Risk Model)是一种处理多种潜在结局生存数据的分析方法,早在1999年Fine和Gray就提出了部分分布的半参数比例风险模型,通常使用的终点指标是累积发生率函数(Cumulative incidence function,CIF)[1-2]。本例中可以将发生AD前死亡作为AD的竞争风险事件,采用竞争风险模型进行统计分析。竞争风险的单因素分析常用来估计关心终点事件的发生率,多因素分析常用来探索预后影响因素及效应值。
2. 案例分析
2.1 [案例分析]
本案例数据来自http://www.stat.unipg.it/luca/R/。有研究者探讨骨髓移植对比血液移植治疗白血病的疗效,结局事件定义为“复发”,某些患者移植后不幸因为移植不良反应死亡,那这些发生移植相关死亡的患者就无法观察到“复发”的终点,也就是说“移植相关死亡”与“复发”存在竞争风险。故采用竞争风险模型分析[3-4]。
首先从当前工作路径中导入数据文件’bmtcrr.csv’。
- library(foreign)
- bmt <-read.csv('bmtcrr.csv')
- str(bmt)
- ## 'data.frame': 177 obs. of 7 variables:
- ## $ Sex : Factor w/ 2 levels "F","M": 2 1 2 1 1 2 2 1 2 1 ...
- ## $ D : Factor w/ 2 levels "ALL","AML": 1 2 1 1 1 1 1 1 1 1 ...
- ## $ Phase : Factor w/ 4 levels "CR1","CR2","CR3",..: 4 2 3 2 2 4 1 1 1 4 ...
- ## $ Age : int 48 23 7 26 36 17 7 17 26 8 ...
- ## $ Status: int 2 1 0 2 2 2 0 2 0 1 ...
- ## $ Source: Factor w/ 2 levels "BM+PB","PB": 1 1 1 1 1 1 1 1 1 1 ...
- ## $ ftime : num 0.67 9.5 131.77 24.03 1.47 ...
这是一个数据框结构的数据,含有7个变量,共177个观测。
$ Sex : 因子变量,2个水平:“F”,“M”。
$ D : 因子变量,2个水平:“ALL(急性淋巴细胞白血病)”,“AML(急性髓系细胞白血病)”。
$ Phase : 因子变量,4个水平:“CR1”,“CR2”,“CR3”,“Relapse”。
$ Age : 年龄。
$ Status: 结局,0=删失,1=复发,2=竞争风险事件。
$ Source: 因子变量,2个水平:“BM+PB(骨髓移植+血液移植)”,“PB(血液移植)”。
$ ftime : 时间。
加载竞争风险模型的程辑包cmprsk,加载数据框bmt,并定义结局为因子变量。
- library(cmprsk)
- ## Loading required package: survival
- bmt$D <- as.factor(bmt$D)
- attach(bmt)
2.2 Fine-Gray检验(单因素分析)
类比两组生存资料log-rank检验,考虑竞争风险事件,同样可以进行单因素分析与多因素分析。下面我们就可以使用cuminc()函数进行单因素的Fine-Gray检验。
- fit1 <- cuminc(ftime,Status,D)
- fit1
- ## Tests:
- ## stat pv df
- ## 1 2.8623325 0.09067592 1
- ## 2 0.4481279 0.50322531 1
- ## Estimates and Variances:
- ## $est
- ## 20 40 60 80 100 120
- ## ALL 1 0.3713851 0.3875571 0.3875571 0.3875571 0.3875571 0.3875571
- ## AML 1 0.2414530 0.2663827 0.2810390 0.2810390 0.2810390 NA
- ## ALL 2 0.3698630 0.3860350 0.3860350 0.3860350 0.3860350 0.3860350
- ## AML 2 0.4439103 0.4551473 0.4551473 0.4551473 0.4551473 NA
- ##
- ## $var
- ## 20 40 60 80 100
- ## ALL 1 0.003307032 0.003405375 0.003405375 0.003405375 0.003405375
- ## AML 1 0.001801156 0.001995487 0.002130835 0.002130835 0.002130835
- ## ALL 2 0.003268852 0.003373130 0.003373130 0.003373130 0.003373130
- ## AML 2 0.002430406 0.002460425 0.002460425 0.002460425 0.002460425
- ## 120
- ## ALL 1 0.003405375
- ## AML 1 NA
- ## ALL 2 0.003373130
- ## AML 2 NA
结果解读:
第一行统计量=2.8623325, P=0.09067592,表示在控制了竞争风险事件(即第二行计算的统计量和P值)后,“ALL”和“AML”累计复发风险无统计学差异P=0.09067592。
$est表示估计的各时间点“ALL”和“AML”组的累计复发率与与累计竞争风险事件发生率(分别用1和2来区分,与第一行第二行一致)。
$var表示估计的各时间点“ALL”和“AML”组的累计复发率与与累计竞争风险事件发生率的方差(分别用1和2来区分,与第一行第二行一致)。
下面我们画出累计复发率与累计竞争风险事件发生率的生存曲线,直观表示上述数字化结果。
- plot(fit1,xlab = 'Month', ylab = 'CIF',lwd=2,lty=1,
- col = c('red','blue','black','forestgreen'))
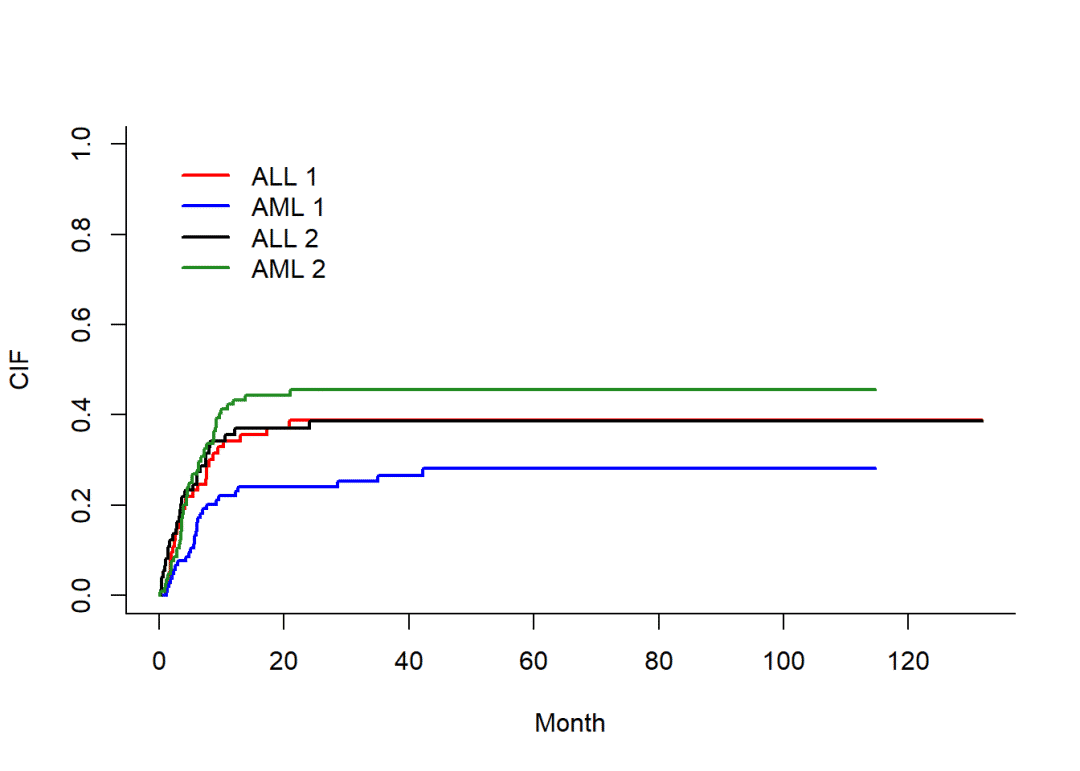
图形解读:
纵坐标表示累计发生率CIF,横坐标是时间轴。我们从ALL1对应的红色曲线和AML1对应的蓝色曲线可以得出,ALL组的复发风险较AML 组高,但未达到统计学意义,P=0.09067592。同理,ALL2对应的黑色曲线在AML2对应的草绿色曲线下方,我们可以得出,ALL组的竞争风险事件发生率较AML组低,同样未达到统计学意义,P=0.50322531。从曲线上不难看出,在前20个月内,各条曲线“纠缠”在一起,所以并未得到有统计学意义的结果。简单来讲,这个图可以用一句话来概括:在控制了竞争风险事件后,“ALL”和“AML”累计复发风险无统计学差异P=0.09067592。
2.3 竞争风险模型(多因素分析)
下面我们进行考虑竞争风险事件的生存资料的多因素分析方法。在cmprsk包中,crr()函数可以很方便的实现多因素分析。该函数的用法如下:
crr(ftime, fstatus, cov1, cov2, tf, cengroup, failcode=1, cencode=0, subset, na.action=na.omit, gtol=1e-06, maxiter=10, init, variance=TRUE)
各参数具体解释各位可以参考crr()函数的帮助文档。此处需要说明的是,该函数必须指定时间变量与结局变量,然后传入协变量矩阵或数据框。首先定义进入模型的协变量,并定位为数据框的形式。
- cov <- data.frame(age = bmt$Age,
- sex_F = ifelse(bmt$Sex=='F',0),
- dis_AML = ifelse(bmt$D=='AML',0),
- phase_cr1 = ifelse(bmt$Phase=='CR1',0),
- phase_cr2 = ifelse(bmt$Phase=='CR2',0),
- phase_cr3 = ifelse(bmt$Phase=='CR3',0),
- source_PB = ifelse(bmt$Source=='PB',0)) ## 设置哑变量
- #cov
构建多因素的竞争风险模型。此处需要指定failcode=1, cencode=0, 分别代表结局事件赋值1与截尾赋值0,其他赋值默认为竞争风险事件2。
- fit2 <- crr(bmt$ftime, bmt$Status, cov, failcode=1, cencode=0)
- summary(fit2)
- ## Competing Risks Regression
- ##
- ## Call:
- ## crr(ftime = bmt$ftime, fstatus = bmt$Status, cov1 = cov, failcode = 1,
- ## cencode = 0)
- ##
- ## coef exp(coef) se(coef) z p-value
- ## age -0.0185 0.982 0.0119 -1.554 0.1200
- ## sex_F -0.0352 0.965 0.2900 -0.122 0.9000
- ## dis_AML -0.4723 0.624 0.3054 -1.547 0.1200
- ## phase_cr1 -1.1018 0.332 0.3764 -2.927 0.0034
- ## phase_cr2 -1.0200 0.361 0.3558 -2.867 0.0041
- ## phase_cr3 -0.7314 0.481 0.5766 -1.268 0.2000
- ## source_PB 0.9211 2.512 0.5530 1.666 0.0960
- ##
- ## exp(coef) exp(-coef) 2.5% 97.5%
- ## age 0.982 1.019 0.959 1.005
- ## sex_F 0.965 1.036 0.547 1.704
- ## dis_AML 0.624 1.604 0.343 1.134
- ## phase_cr1 0.332 3.009 0.159 0.695
- ## phase_cr2 0.361 2.773 0.180 0.724
- ## phase_cr3 0.481 2.078 0.155 1.490
- ## source_PB 2.512 0.398 0.850 7.426
- ##
- ## Num. cases = 177
- ## Pseudo Log-likelihood = -267
- ## Pseudo likelihood ratio test = 24.4 on 7 df,
结果解读:在控制了竞争分险事件后,phase变量,即疾病所处阶段是患者复发的独立影响因素。以relapse阶段的患者为参照,CR1, CR2, CR3的累计复发分险较Relapse阶段的患者,HR及95% CI分别为0.332(0.159,0.695), 0.361(0.180,0.724), 0.481(0.155 1.490), 对应的P值分别为0.0034, 0.0041, 0.2000。
3. 讨论和总结
本文详细介绍了使用R的cmprsk程辑包进项Fine-Gray检验与竞争风险模型。笔者认为读者在具体应用过程中要注意两点:
第一,有选择性的使用Fine-Gray检验与竞争风险模型,如果终点事件存在竞争风险事件,而且极有可能对结论产生影响,那采用这个模型才是合适的,这个模型并非一定比Cox模型更优,这两个模型应该互为补充;
第二,竞争风险考虑的竞争风险事件也是有限的,目前仅是把Cox模型的二分类终点扩展为三分类,即结局事件,删失和竞争风险事件,即便如此,结果解读也变得很困难。读者在方法选择的时候应该做出更充分的评估和尝试。
4. 参考文献
[1].Fine JP and Gray RJ (1999) A proportional hazards model for the subdistribution of a competing risk. JASA 94:496-509.
[2].Gray RJ (1988) A class of K-sample tests for comparing the cumulative incidence of a competing risk, ANNALS OF STATISTICS, 16:1141-1154.
[3].Scrucca L., Santucci A., Aversa F. (2007) Competing risks analysis using R: an easy guide for clinicians. Bone Marrow Transplantation, 40, 381-387.
[4].Scrucca L., Santucci A., Aversa F. (2010) Regression modeling of competing risk using R: an in depth guide for clinicians. Bone Marrow Transplantation, 45, 1388–1395.


