单细胞测序技术自2009年问世,2013年被Nature Methods评为年度技术以来,越来越多地被应用在科研领域。
2015年以来,10X Genomics、Drop-seq、Micro-well、Split-seq等技术的出现,彻底降低了单细胞测序的成本门槛。
自此,单细胞测序技术被广泛应用于基础科研和临床研究。单细胞在许多领域都占有一席之地,对于癌症早期的诊断、追踪以及个体化治疗具有重要意义。
1
为什么要做单细胞测序?
初次听说单细胞测序技术,单细胞测序又是什么噱头?如果单细胞测序就能测一个细胞或几个细胞的话,这有什么意义?特别是对异质性高的肿瘤组织来讲,测一个细胞能代表什么?
无论是蠕虫,蓝鲸,还是人类,自然界所有的多细胞生命都是从单个细胞发育而来开始。
这样一个单细胞,鬼斧神工地构建出有机生命体所需的各种组织、器官、系统。每个新细胞在正确的时间,在正确的地方分裂、分化,并与相邻细胞协调精准发挥功能。
多细胞生命的发育过程,是自然界中最引人注目的壮举之一。尽管经过数十年的研究,生物学家仍然无法完全理解这一过程。
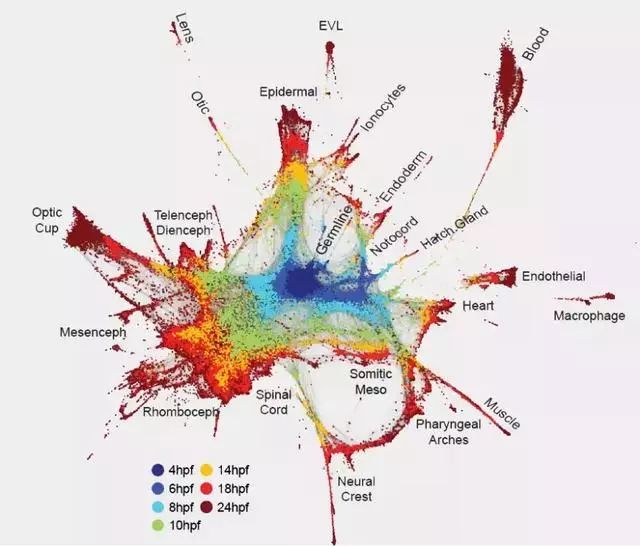
2018 年 4 月 26 日,Science 杂志发表三篇超重磅研究,来自哈佛医学院和哈佛大学的研究人员使用多种技术组合,包括对发育中斑马鱼和青蛙胚胎数千个单细胞的基因测序,以精确的方式跟踪和描绘了组织和整个机体从单细胞发育的完整历程。
哈佛大学分子和细胞生物学教授 Alexander Schier 表示,“这几乎就像通过几颗星星看到了整个宇宙。”
使用单细胞测序技术,研究团队在胚胎发育的最初 24 小时内追踪单个细胞的命运,揭示出单个细胞基因开启或关闭的综合景观,以及胚胎细胞何时何地转变为新的细胞状态和类型。
这些发现就好比是勾勒出胚胎发育过程中产生不同细胞类型的遗传“配方”目录,为发育生物学的深入研究和疾病的认识,提供了前所未有的资源。
图 | 斑马鱼受精卵在 4、6、8、10...... 小时(hpf)时的发育过程中不同器官细胞形成,最中心的深蓝色为受精卵,以时间为单位向外辐射。
“通过单细胞测序,我们可以在一天的时间里概括数十年来对细胞在生命早期阶段分化的艰苦研究。”哈佛医学院系统生物学助理教授 Allon Klein 表示,“通过我们开发的方法,我们正在绘制我们认为发育生物学的未来,发育生物学将会转变为定量的、大数据驱动的科学。”
Alexander Schier 表示,除了对生命早期阶段有所了解之外,这项工作还可以为大量疾病的新认识打开大门。“我们预见,任何复杂的生物学过程,只要是细胞随时间改变了基因表达,都可以使用这种方法重建,不仅仅是发育中的胚胎,还有癌症发生或大脑退化。”
2
基本原理
单细胞测序首先不是仅仅对一个细胞进行测序,而是说该项技术能对单一细胞的基因组或转录组进行测序,可以理解为单细胞水平上的测序。
在介绍基本原理之前先让我们尝试着回答一下:为什么要进行单细胞测序?换个姿势来问就是,单细胞测序技术能解决什么传统方法解决不了的问题?
世界上没有两片相同的叶子,对于多细胞生物来说细胞与细胞之间是存在差异的,很多时候是基因组、转录组上的失之毫厘,功能上的差之千里。
比如在肿瘤组织中,肿块中心的细胞与肿块周围的细胞,原发灶与转移灶的细胞,其基因组与转录组等遗传信息是存在差异的,这也就导致不同肿瘤细胞表现出免疫特性、生长速度、侵袭能力等表型方面的差异,最终导致对不同抗肿瘤药物的敏感性不同或放疗敏感性的差异。
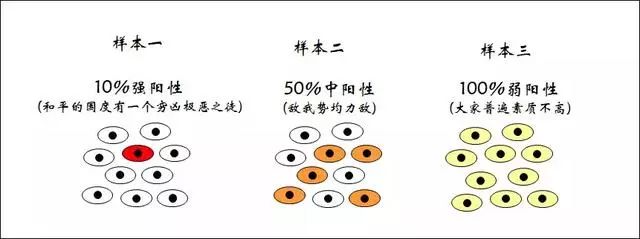
那么我们怎样来研究这种遗传信息的异质性呢?传统的测序方法是在多细胞水平上进行的,这种大家一起“吃大锅饭”的形式,使其丢失了异质性的信息,而单细胞测序可以完美的解决这个问题。给大家更形象的举个例子:
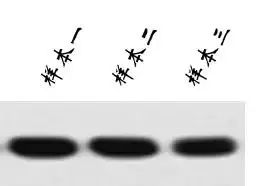
Western blot 检测
这三种样本虽然存在这么大的差异,但是通过western blot检测的时候我们得出的结论是:该基因在不同组织中的表达基本一致。上图所展示的异质性信息就被完全的忽略掉了。
和western blot相似的是,传统测序方法所展示的信息也是在多细胞水平上的平均信息,而单细胞水平上的测序则完全可以反应同一个细胞群里不同细胞的基因组和转录组状况。
单细胞测序技术的出现,使得从混杂的样品中筛选出异质性信息的难题得以解决,该技术的成熟使用也必将引领生命科学研究向前迈进一大步。
那么单细胞测序又是如何实现的呢?我们以单细胞RNA-seq作为例子,简单的来介绍一下该技术得以实现的原理:
一,将单细胞分离出来,单独构建测序文库,并进行测序。这种思路通量极低而且成本极高,如前文所说烧掉很多钱就测数十个细胞,而往往这数十个细胞还不足以反应真实的科学问题。所以我们着重介绍第二种方案。
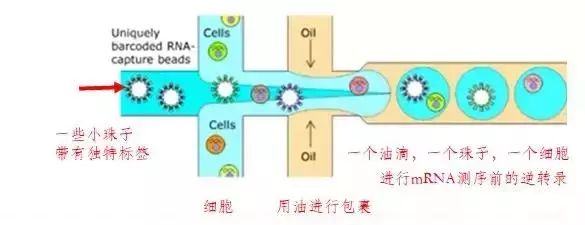
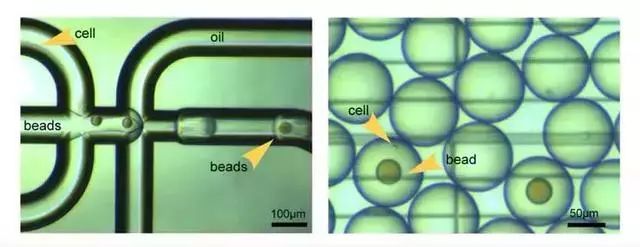
二,基于标签(barcode)的单细胞识别。它的核心思想是:在对每个细胞的mRNA测序前做逆转录时,为其加上独一无二的标签序列。这样即便是混合起来测序,我们也可以把携带相同标签序列(barcode)的RNA片段视为来自同一个细胞。通过这种策略,我们可以通过一次建库,测得上万个单细胞的信息(如下图所示)。
3
单细胞测序带给大家哪些福利?
就拿大家比较关注的single cell RNA-seq来说吧:
一、在传统的研究方法中,我们往往根据标记基因和细胞形态来区分不同细胞类型,而这种方法无可厚非的存在很多争议。而单细胞测序技术可以更精准无偏倚的来对细胞进行分群。尤其是对免疫学,肿瘤学,遗传学的研究将会带来巨大影响。
二、分析稀有的细胞,特别是特定时空环境下的细胞。比如从环境中取样的微生物等。
三、临床上,对体外受精胚胎进行植入前的筛查。
四、基于循环肿瘤细胞(circulating tumor cells)进行癌症诊断,大力推进新型的循环肿瘤细胞检测技术。特别是恶性肿瘤患者治疗前后的循环肿瘤细胞类型和数量的变化具有重要的预后提示价值。
五、已经通过传统的测序方法进行大规模测序,希望以此挖掘数据冲击重量级期刊的小伙伴们请注意,单细胞测序在高分期刊的发表已成井喷之势,几年之后技术必将更加成熟。
4
单细胞测序技术的应用
单细胞测序技术助力肿瘤研究
1.Cell:以色列研究团队使用单细胞转录组测序揭示黑色素瘤肿瘤浸润T细胞的转录组异质性和分化途径。
以色列Ido Amit实验室李汉杰博士等发现,癌症中免疫细胞的异质性对免疫治疗的效果有重要影响,功能失调的CD8 T细胞在肿瘤微环境中处于动态分化和高度活跃的状态,而且很可能驱动着肿瘤特异性免疫应答。
该团队通过对25名黑色素瘤患者肿瘤中免疫细胞,进行单细胞转录组测序和单细胞TCR测序分析,绘制黑色素瘤详尽的免疫细胞图谱。
该研究发现尽管不同免疫细胞亚型存在于大多数患者中,但是它们的相对丰度在不同患者中存在很大差异。此外,尽管丰度不同,所观察到的CD8T细胞的分化途径却是高度保守的。该研究为癌症中免疫细胞的异质性对免疫治疗的效果进一步提供了理论支撑。
2:Nature,Nature Medicine两连发:北京大学张泽民教授课题组重磅解析结直肠癌和肺癌免疫微环境
张泽民教授课题组分别在《Nature Medicine》和《Nature》发布重大研究成果,在单细胞水平绘制肺癌和结直肠癌T细胞免疫图谱,揭示了肺癌和结直肠癌T细胞的亚群分类、组织分布特征、肿瘤内群体异质性及药物靶基因表达情况,鉴定了跨组织分布的T细胞类群及亚群间潜在的状态转换关系,这对于肺癌和结直肠癌的诊断和治疗具有重大意义。
该团队将继续利用单细胞测序技术和生物信息方法结合,来阐明肿瘤微环境特别是肿瘤浸润免疫细胞的精确组成和功能状态,探究肿瘤内部各类细胞的特异属性、相互关系、及动态变化,从而找到新靶点,开拓克服肿瘤的新颖方法。
3:Cell:美国研究团队绘制目前规模最大免疫细胞图谱,探索乳腺癌免疫微环境
美国Sloan Kettering癌症中心团队,使用单细胞转录组测序技术,分析了人乳腺肿瘤以及配对的正常乳腺组织,外周血和淋巴结4个组织来源的共47016个免疫细胞的基因表达特征。揭示肿瘤内淋巴细胞和髓系细胞的异质性,与正常乳腺组织相比显著的表型扩增。这种异质性通过各种环境刺激反应引起的组合基因的表达,且TCR的特异性参与了T细胞组合基因表达的形成。所观察到的T细胞状态的连续性变化颠覆了之前较少分化或激活离散状态形成的肿瘤微环境经典概念。
单细胞转录组分析与心脏病
Cell Stem Cell:从单细胞水平描绘了人心肌细胞重编程过程中转录组随着细胞命运转化而发生的改变。
该论文由来自北卡罗来纳大学(UNC)的心肌细胞重编程领域开创者之一钱莉教授带领的研究团队发表。研究人员首先报道了优化的人心肌细胞重编程的方法,利用最精简的重编程因子达到了高效的重编程效果(~50%的转化细胞表达心肌细胞的标记分子cTnT)。
研究人员利用单细胞测序详细描绘了人心肌细胞重编程过程中转录组的动态变化和细胞命运的二项选择,即在成纤维细胞向心肌转化的早期诱导阶段存在一个“决策点”,决定了细胞的命运能否成功地被转化。
除了描绘整体的重编程图谱外,通过深度挖掘单细胞转录组数据,该研究还为进一步了解人心肌细胞重编程的分子机制提供了大量的线索和研究方向。基于重编程响应和非响应途径的差异基因比对,研究人员还找到了正向和反向的分子标记物,将来可用于筛选和富集转化的心肌细胞。
单细胞转录组分析阿尔茨海默病
Nature:单细胞转录组分析阿尔兹海默病
来自美国麻省理工学院的研究人员首次对阿尔茨海默病患者的单个脑细胞中表达的基因进行了综合分析。所获得的分析结果允许他们鉴定出在神经元和其他类型的脑细胞中受到影响的独特细胞通路。这一分析可能为阿尔茨海默病提供许多潜在的新型药物靶点。
研究人员分析了24名表现出高水平阿尔茨海默病病理学特征的人和24名具有相似年龄的没有这些疾病迹象的人的尸检大脑样本,对来自这些受试者约8万个细胞进行单细胞RNA测序。通过该测序技术,研究者不仅能够分析最丰富的细胞类型,包括兴奋性和抑制性神经元,而且还能分析稀有的非神经元脑细胞,如少突胶质细胞、星形胶质细胞和小胶质细胞。
研究发现,这些细胞类型中的每一种在阿尔茨海默病患者中都表现出明显的基因表达差异。在患有阿尔茨海默病的个体中,与髓鞘形成相关的基因在神经元和少突胶质细胞(产生髓鞘的细胞)中都受到影响。
单细胞测序与糖尿病
Nature:Chartingcellular identity during human in vitro β-cell differentiation
哈佛大学干细胞研究所的Douglas A. Melton团队,使用单细胞测序的方法,详细地分析了诱导方案中细胞组成和基因表达动态变化;并发现CD49a(ITGA1)是β细胞的表面标记物,可用来富集β细胞;同时,也为研究体内胰腺祖细胞分化为胰岛细胞过程提供指导。
单细胞测序发现新的肠道干细胞
Nature:Single-cell tranomes of the regenerating intestine reveal a revival stem cell
加拿大西奈山医院的Alex Gregorieff和Jeffrey L. Wrana领导的研究团队,发现了一类独特的干细胞,其会在小肠受损伤后激活以维持干细胞池稳态并促进小肠上皮再生。这类新的小肠干细胞——revSCs,revSCs是一种缓慢循环的细胞类型,受YAP1信号调控后出现在受损的肠道中,以重建LGR5+ CBCs干细胞池,促进肠道再生。因此,损伤引起的revSCs扩增可能是小肠损伤修复的关键机制。