临床研究有四大原则:随机、对照、盲法、重复。我们对随机、对照、盲法非常熟悉,但重复验证究竟有多重要?重复验证原则会不会是为了凑个“四”自己加上去的?相信这么想的人还不在少数。那我们今天就来讨论一下“重复”这个原则。
虽然,我们都希望自己研究有创新,甚至现在无论写标书或者研究生毕业也必须提创新点。但我们必须要讲,在临床研究中,重复是必不可少的,只有可以被重复验证的研究结果才是真实存在的规律。重复这一条尤其在临床研究中,更需要被重视。因为临床研究环境太复杂,可能影响研究结果的因素太多了,很难保证每个临床研究的结果一定揭示了真实的规律。而假如有偏差的临床研究结果应用到临床实践中,则可能带来严重的影响。我们来看看新药研发的过程,其实里面就隐含这重复这个原则。I期试验是新药首次在人体中应用,目标是探索药物的药代、药动特征,初步了解安全性指标;II期是在病人中使用药物,初步探索有效性以及剂量效应、剂量反应关系;III期是药物有效性的验证;即使上市后,可能还需要开展IV期试验来进一步验证有效性和探索安全性问题。也就是说在药物上市前、上市后需要进行多次重复研究,目标只是为了证明某个药物安全有效。甚至很多研究者认为仅仅根据这些药物临床试验的结果不足以确证药物确实安全有效,还需要更多的重复。
一篇即将在Journalof clinical epidemiology 11月刊上的文章专门讨论RCT结果是否会overestimate药物的效果。文中用了type S error,即真实情况是试验组药物疗效更好,试验得到却是对照组更好的结果的可能性,或者反之真实情况是对照组更好,但研究结果却指示试验组更好的可能性。我们来刊其中一部分的结果:
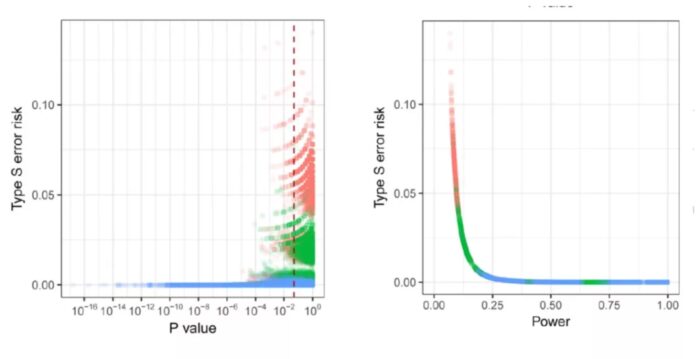
图中显示的就是typeS error的风险随着临床试验数据的变化,其中红色点指示的是组间OR为1.3,绿色是1.5,蓝色是2;相通颜色的点中,位置最高到最低是样本量为每组50、100、200、300、400、500的情况。作者一共进行了3600次的模拟得到了上面的两张图。也就是当p值越大,样本量越小的时候,得到研究结果和真实结果偏离的风险越高,而在研究power不足的情况下,也更容易得到偏离真实情况的研究结果。
基于以上的数据,我们知道即使是RCT试验中,若仅靠某次结果来下一个确定性的结果,我们犯错误的风险还是很高的。其实也就是说,研究结果应进行多次重复,当重复的研究结果越一致,说明研究结果的稳定性越好。


