1、单细胞测序概论
过去二十几年里,随着基因测序技术水平的提高以及千人基因组计划、癌症基因组计划、Meta-Hit计划等重大国际合作项目的相继开展,基因组研究日渐被推向高潮。然而,迄今为止使用的测序材料无一例外都是数百万甚至更多细胞的混合DNA样本。这种方法能够得到全基因组序列信息,但是对其进行研究得到的结果只是一群细胞中信号的平均值,或者只代表其中占优势数量的细胞信息,单个细胞独有的特性被忽视。例如,科学家想找出哪种突变存在于哪种细胞中几乎是不可能的,只存在于少数细胞(如早期癌细胞)中的突变也基本上被掩藏。另一方面,有些样品稀少无法在实验室培养,样品量不足以进行全基因组分析,例如肿瘤循环细胞、组织微阵列、早期发育的胚胎细胞等。这些都是全基因组测序遇到的难题。
作为“在单个细胞水平上对基因组进行测序”的单细胞测序技术能够解决上述难题。与传统的全基因组测序相比,单细胞测序不仅测量基因表达水平更加精确,而且还能检测到微量的基因表达子或罕见非编码RNA,其优势是全方位和多层次的。
2011年,《自然方法》杂志( Nature Methods )将单细胞测序列为年度值得期待的技术之一[1],2013年,《科学》杂志(Science)将单细胞测序列为年度最值得关注的六大领域榜首[2]。与此同时,测序巨头相继推出新一代测序仪,为单细胞测序提供利器,越来越多与单细胞测序有关的研究也发表在顶级期刊上,这些都表明,单细胞测序已逐渐成为科研热点,有望成为2013年最值得关注的测序技术。
2、单细胞测序基本路线
近年来,流式细胞分选和激光捕获显微切割技术的出现让单细胞的捕获成为可能。单细胞测序技术正逐渐从实验研究方法成为指导临床的有利工具,为基础研究向临床转化搭建了桥梁。单细胞测序主要涉及单细胞基因组测序和转录组测序两方面,分别针对单个细胞的DNA和RNA进行序列分析和比较,进而揭示基因组和转录组的变化。
2.1、单细胞全基因组测序
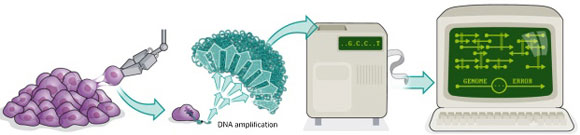
单细胞全基因组测序技术是在单细胞水平对全基因组进行扩增与测序的一项新技术。其原理是将分离的单个细胞的微量全基因组DNA进行扩增,获得高覆盖率的完整的基因组之后通过外显子捕获进而高通量测序用于揭示细胞群体差异和细胞进化关系。
全基因组扩增技术主要分为两种类型:一是基于热循环以PCR为基础的扩增技术,如简并寡核苷酸引物PCR (DOP-PCR)、连接反应介导的PCR (LM-PCR)、扩增前引物延伸反应 (PEP)等;一是基于等温反应不以PCR为基础的扩增技术,如多重置换扩增 (MDA) 和基于引物酶的全基因组扩增 (pWGA)。
在这两种类型中,PCR扩增比较经典,但是,对不同的序列来说,PCR扩增的效率存在相当大的偏差,易产生扩增偏倚问题: 如富含CG的DNA序列和相应基因座位的非随机丢失,等位基因的非随机丢失,以及与DNA片段大小相关的偏差(倾向于扩增更多短片段),尤其是在应用于单细胞时,大量短片段导致片段间序列丢失,从而使其应用受限。
MDA是目前公认的最好的单细胞基因组扩增技术,它能对全基因组进行高保真的均匀扩增,扩增出10~100kb大小的片段,能提供大量均一完整的全基因组序列。但是MDA也有一些缺点,特别是显著的非特异扩增,往往空白对照样品也总是“无中生有”地产生大量的DNA,另外就是仍然存在序列偏差。尽管各种改进的策略正在逐步减少这些缺陷,高覆盖率、高保真性及高特异性的扩增仍然是亟待解决的问题。另外,对测序得到 的大量数据结果的专业分析也是一个重大的挑战。 单细胞全基因组测序正在从基础研究走向临床应用。
2.2、单细胞转录组测序
单细胞转录组分析主要用于在全基因组范围内挖掘基因调节网络,尤其适用于存在高度异质性的干细胞及胚胎发育早期的细胞群体。与活细胞成像系统相结合,单细胞转录组分析更有助于深入理解细胞分化、细胞重编程及转分化等过程及相关的基因调节网络。将此技术应用于临床,理论上可以在生理 或病理情况下连续追踪基因表达的动力学变化,从而监测疾病的进展。单细胞转录组分析的另一应用领域是发现亚细胞成分的基因表达谱,例如对在神经元的轴突或树突部分特异表达的基因的转录组的分析,这些基因往往对细胞的生物学功能发挥着重要作用。但是,鉴于目前的技术手段,单细胞转录组测序仍然存在覆盖率低的弊端,导致除mRNA以 外的长非编码RNAs难以检测,并且不能区分正义链与反义链。最近发展的单分子测序技术无需逆转录和扩增步骤而直接对单个细胞的全长mRNAs进 行测序,从而准确地检测基因不同的剪切亚型的表达水平。随着技术的发展这些局限性会被逐步优化和改进。
3、单细胞测序技术实例
 3.1、多重退火和成环循环扩增技术(Multiple Annealing and Looping-Based Amplification Cycles, MALBAC)
3.1、多重退火和成环循环扩增技术(Multiple Annealing and Looping-Based Amplification Cycles, MALBAC)
主要研发人:哈佛大学终身教授、美国科学院院士谢晓亮(Sunney Xie)教授
技术看点:降低PCR扩增偏倚,使得单细胞中93%的基因组能够被测序。这种方法使得检测单细胞中较小的DNA序列变异变得更容易,因此能够发现个别细胞之间的遗传差异。这样的差异可以帮助解释癌症恶化的机制,生殖细胞形成机制,甚至是个别神经元的差异机制。
技术简介:
PCR扩增具有偏好型而且基因组具有大量的冗余,造成了基因组测序准确性不高。
谢晓亮研发的MALBAC技术能从一个细胞的基因组中,分离出来自单细胞的DNA,然后添加称作引物的短DNA分子。这些引物可与DNA的随意部分互补,从而使得它们能够附着到DNA链上,充当DNA复制起点。
这些引物由两个部分构成——一个包含8个核苷酸的粘性部分变化多样,可与DNA结合,再加上一个包含27个核苷酸的共同序列。这一共同序列可防止DNA太多次拷贝,大大地降低了扩增偏倚。通过将自身掺入到新拷贝链,从而自身成环,防止了过度拷贝。利用这种方法,进行与加入的引物的DNA复制时,可以完成高达93%的基因组测序。
技术论文:Genome-Wide Detection of Single-Nucleotide and Copy-Number Variations of a Single Human Cell
3.2、基于芯片实验室技术的单细胞测序
主要研发人:斯坦福大学Stephen Quake
技术看点:基于lab on a chip开发
技术简介:
本技术设计了一种路线,用液体载运细胞通过一连串显微管道和微阀门,当细胞挨个进入各自的小空位时,它们的DNA就会被提取出来,经过复制用于进一步分析。
此外,本技术不仅能分离细胞,还能用化学试剂将细胞混合起来,通过检测反应过程中的荧光发射获得它们的基因编码。所有这些都能在芯片上完成,不仅操作简单,而且成本效益高。
Stephen Quake已利用此技术完成了第一例人类单细胞测序,现在他正利用这项技术研究精子细胞中的重组并分析突变率。
技术论文:Genome-wide Single-Cell Analysis of Recombination Activity and De Novo Mutation Rates in Human Sperm
3.3、基于MDA的单细胞测序
主要研发人:深圳华大基因研究院
技术看点:将多重置换扩增(MDA)和测序技术相结合。
技术简介:
本技术基于多重置换扩增(MDA),并对该方法的扩增均一性、灵敏度、特异性等方面进行了全面评估。这种将多重置换扩增和测序技术相结合的单细胞测序方法不仅具有更高的分辨率和基因组覆盖度,而且具有更好的敏感性和特异性。该方法从单核苷酸水平上为各种复杂疾病和生物学过程的研究开辟了新思路。
技术论文:Single-Cell Exome Sequencing and Monoclonal Evolution of a JAK2-Negative Myeloproliferative Neoplasm
Single-Cell Exome Sequencing Reveals Single-Nucleotide Mutation Characteristics of a Kidney Tumor
3.4、Strand-seq
主要研发人:加拿大英属哥伦比亚大学Peter Lansdorp
技术看点:能捕捉DNA一条链上的信息,使得研究人员能对亲本DNA模板链进行单细胞测序,避免单细胞DNA扩增和测序时丢失定向信息。
技术简介:
在细胞分裂过程中,当双螺旋解旋后,两条染色体上的遗传信息偶然会出现交换,如果这样的交换水平不断提高,就标志着出现了DNA损伤和癌症。传统的基因组测序,由于在单细胞DNA扩增和测序的时候,会丢失定向信息,难以检测到基因重排,因此也就检测不出这一点。
Strand-seq方法能分别对单细胞的双亲DNA模板链进行测序,获得高分辨率的姊妹染色体交换图谱,检测到基因重排,从而发现细胞复制过程中,DNA序列的翻转或交换。
利用Strand-seq方法,研究人员完成了单链DNA测序,并发现了首个基因组压力和不稳定性的痕迹。
技术论文:DNA template strand sequencing of single-cells maps genomic rearrangements at high resolution
4、单细胞测序应用案例及成果
单细胞测序解决了用组织样本测序时或样本少无法解决的细胞异质性难题,为从单核苷酸水平深入研究癌症发生、发展机制及其诊断、治疗提供了新的研究思路并开辟了新的研究方向。此外,这一新方法还可被广泛用于其他重要的生物研究领域,如组织器官内细胞基因组的异质性研究、干细胞的异质性研究、生殖细胞的遗传重组研究、胚胎的植入前遗传学诊断研究、法医学少量DNA测序等。
不过,就目前来说,单细胞测序最常见的应用是在癌症研究上。由于癌细胞中基因组部分被删除,或者扩增,从而引起关键基因的缺失,或者表达过量,干扰正常细胞生长,因此利用这种方法就能分析基因拷贝数目,从而诊断癌症。以下列出了单细胞测序常应用的领域。
4.1、肿瘤单细胞测序
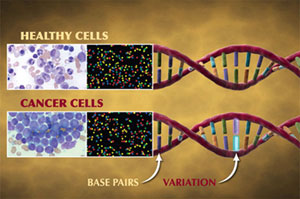
已有的研究表明,基因或基因组变异是肿瘤发生的根本原因,利用单细胞全基因组测序技术,可以对获取的肿瘤细胞进行更为精确和深入的分析,发现正常细胞与肿瘤细胞差异,了解癌细胞的基因如何突变,以及肿瘤的来源、肿瘤的生长规律、属于哪种基因型等,为早期检测和诊断肿瘤和肿瘤的个体化治疗提供指导。另外,肿瘤的异质性是导致肿瘤耐药性问题的原因。如果 能从单个肿瘤细胞水平对肿瘤单细胞进行测序,并 找出一个肿瘤在单个细胞上的共同结构,揭露出每个肿瘤细胞的突变规律,这将为药物研究、肿瘤的靶向治疗提供基础。
2008年,美国华盛顿医学院的Ley等完成了对一位50多岁死于急性骨髓性白血病(acute myeloid leukemia, AML)的患者的基因组测序工作。他们利用高级流式细胞术分离出细胞表面CD13、CD33和CD117阳性,但CD34阴性的肿瘤细胞,并检测它的遗传突变。 最终在患者的肿瘤 DNA中仅发现了10个可能与AML有关的遗传突变, 其中8个很罕见,这也是首次发现的与AML有关的基因。通过单细胞分析技术,测得每个肿瘤样本细胞拥有9个突变[3]。
2011年,Navin等利用DOP全基因组扩增及DNA测序对单个乳腺癌细胞进行了拷贝数变异的分析,进而推断出细胞的群体结构和肿瘤的进化过程。但是由于该方法的基因覆盖率较低,而且不能在单个核苷酸的分辨率上评价单个肿瘤细胞的遗传学特征,故并不能检测在肿瘤发展过程中发挥重要作用的单个核苷酸的改变[4]。
2012年,华大基因首次利用以MDA为基础的单细胞测序技术对原发性血小板增多症(essential thrombocythemia, ET)病人的单个骨髓细胞进行了测序并分析,筛查出在ET发病和进展中的驱动基因, 从而证实ET为单克隆来源的疾病[5]。同时,也将该方法与经典方法进行比较,从而建立了具有高敏感性、高特异性、假阳性率低等特点的单细胞测序方法,为分析疾病的遗传学结构特征及克 隆进化过程提供了新的思路。同样的方法也用于分析单个肾癌细胞的单核苷酸突变特征,从而在更高的分辨能力上为评价基因改变的复杂性提供了更为优化的方法[6]。
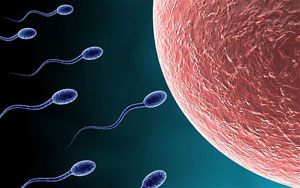
4.2、单生殖细胞测序
单细胞DNA扩增技术和高通量测序技术的发明,使得测序单个生殖细胞的基因组成为可能,利用单细胞全基因组测序技术来研究人类的染色体重组规律,具有以往技术无法比拟的优势。
美国科学院院士、哈佛大学教授谢晓亮课题组与北京大学生物动态光学成像中心(BIOPIC)研究员李瑞强课题组联合起来,将单细胞测序应用到一个单一的亚洲男性精子的DNA测序,结果发现基因区附近重组率的降低由分子机制所决定,而非自然选择的结果,证明这种方法能准确识别单个核苷酸的变化。这项工作首次实现了高覆盖度的单个精子全基因组测序,构建了迄今为止重组定位精度最高的个人遗传图谱,这一技术方法在男性不育症研究和肿瘤早期诊断及个体化治疗等生物医学领域有着广泛的应用前景[7]。
美国斯坦福大学医学中心的研究人员借助单细胞测序技术对源自一名男性的91个精子细胞的全部基因组进行了测序,发现许多新的重组热点和与间接方法发现的相一致的比率。 随后他更深程度地测序了8个精子足以确定突变率。这将有助于学界更加了解自然发生的个体遗传突变,对于不孕不育症的科研具有重要意义[8]。
美国艾伯特爱因斯坦医学院的统计遗传学家Auton在2012年冷泉港的基因组生物学会议上报告说,对近200个精子细胞进行的测序,能够估算出捐精给他们的男子的重组率。该研究工作详细结果还未发布,Auton仅表示,他们发现每个精子细胞平均有24.5个重组事件,与来自间接实验的结果相一致。
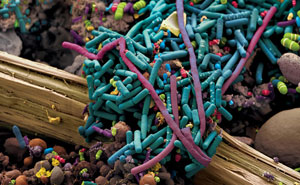
4.3、微生物单细胞测序
人体内和环境中生存着各种微生物,但大部分微生物不能在实验室中培养,这阻碍了研究人员对它们的测序和研究。单细胞测序能够用来深入研究单个细菌细胞的基因组。
来自J. Craig Venter研究所、加利福尼亚大学以及Illumina Cambridge公司的研究人员就尝试着对加利福尼亚海洋样本中的单个细菌——SAR324细胞基因组进行了测序。
研究人员使用的单细胞测序方法利用了多次替换扩增、Illumina GAIIx末端配对测序,以及一种新的能够解决扩增偏向的单细胞装配算法(EULER+Velvet-SC)。他们在大肠杆菌和金黄色葡萄球菌上验证可行性后,随后将研究对象换成SAR324,结果生成了单细胞基因组序列,装配出430万个碱基的contig序列,其中含有3811个开放阅读框,获得了传统全基因组研究中缺少的细胞特异的遗传信息。
尽管还需要进一步研究来弄清SAR324在环境中的作用,但基因组模式表明该细菌是好氧菌,且移动的。结合tRNA、氨基酸和维生素相关基因,研究人员还发现了参与有氧代谢、鞭毛形成及趋化作用的基因。
今后,研究人员计划使用相似的策略对不同环境中的单个细菌细胞进行测序,从大海深处到医院病房及人体内。作者认为,这种经济高效的方法应该有助于微生物分类和进化的探索,且能够挖掘出一些环境微生物,其基因和通路能够为生物技术和生物医学所用[9]。
5、单细胞测序展望
从2011年到2012年,经过了两年迅速的技术演进,单细胞测序吸引了众多研究人员的眼球,但是它还没有取得质的飞跃,仍然处于不成熟的阶段,在技术上和成本上还远没有达到大规模应用的地步。
但是,单细胞测序的前景依然是乐观的。美国马里兰州贝塞斯达美国国家人类基因组研究院(National Human Genome Research Institute in Bethesda, Maryland)的遗传学家Elaine Ostrander说:单细胞基因组测序技术是一种让人难以置信的新技术,这种技术的应用潜力无法估量,我们可以凭借这种技术轻而易举的攻克肿瘤难题。
中国华大基因研究院副院长李英睿说:“单细胞测序新方法为遗传异质性肿瘤的高精度、全面评估提供了一个非常优秀的研究工具。这种新方法和产生的数据为鉴定与肿瘤发展相关的候选基因提供了科学依据,也必将会推动癌症的遗传机理和生物学过程更深入的研究。”
我们有理由相信,在不远的未来,单细胞测序将会把组织器官内细胞基因组的异质性研究、干细胞的异质性研究、生殖细胞的遗传重组研究、胚胎的植入前遗传学诊断研究等领域带入一个前所未有的精致程度,我们将迎来更多革命性的科技进步。
6、参考文献
[2]Single-Cell Sequencing Tackles Basic and Biomedical Questions
[3]DNA sequencing of a cytogenetically normal acute myeloid leukaemia genome
[4]Tumour evolution inferred by single-cell sequencing
[5]Single-Cell Exome Sequencing and Monoclonal Evolution of a JAK2-Negative Myeloproliferative Neoplasm
[6]Single-Cell Exome Sequencing Reveals Single-Nucleotide Mutation Characteristics of a Kidney Tumor
[7]Probing Meiotic Recombination and Aneuploidy of Single Sperm Cells by Whole-Genome Sequencing
[8]Genome-wide Single-Cell Analysis of Recombination Activity and De Novo Mutation Rates in Human Sperm
原文来自:http://www.biodiscover.com/topic/technology/254.html